以“拥抱监管,拥抱变化”為(wèi)主题的IHMD·2024 医疗美容高端器械峰会于2024年4月25日-26日在上海龙之梦大酒店(diàn)举办。

此次会议山(shān)东众山(shān)生物(wù)技术总监王朋田受邀参加,并且在会中发表以《注射级透明质酸钠关键质量指标及应用(yòng)分(fēn)析》為(wèi)题的主题演讲,得到了大家的认同与肯定。

判断透明质酸钠原料质量可(kě)以从以下三个方面考究:
1、杂质以及安全指标,包括核酸、蛋白、还有(yǒu)溶血性链球菌等等,这些指标真正反映了一个原料供应的生产水平。
2、黏度性指标,具體(tǐ)的检测结果更多(duō)是以实测值為(wèi)准,客户在这些指标方面,是对我们有(yǒu)着明确的目标要求,或者定制化生产的需求。这是从另外一个侧面反映了一个原料供应商(shāng)生产上的技术水平。
3、微生物(wù)指标,根据微生物(wù)指标的情况,可(kě)以将现在市面上的产品分(fēn)為(wèi)合格产品以及检测无菌的产品。

哪些因素影响杂质与安全指标、黏度与安全指标,我们可(kě)以从以下四个角度进行思考。
1、从微生物(wù)限度进行思考,产品仅仅是微生物(wù)限度合格,不排除我们粉末里面有(yǒu)微生物(wù)的出现,以及储存、生产、使用(yòng)过程中微生物(wù)的变化。哪怕是检测无菌的产品,也仅代表微生物(wù)的现在检查我们没有(yǒu)检测出来,并不是100%排除微生物(wù)的过程。
2、从湿热灭菌角度进行思考,假如我们做医疗器械过程中有(yǒu)湿热灭菌的环节存在,我们无法将最大的分(fēn)子量带到终端的产品中。我们購(gòu)买的是200万分(fēn)子量产品,结果灭菌就只能(néng)变成100万分(fēn)子量产品。
3、从杂质变化方面思考,我们的产品里面还有(yǒu)经过微生物(wù)限度检测合格,但是还有(yǒu)一点点微生物(wù)存在的情况,经过湿热灭菌,微生物(wù)被杀灭之后,不排除会带来新(xīn)的内毒素的产生。我们也不排除玻尿酸在这其中有(yǒu)其他(tā)的反应。
4、从分(fēn)子量的反应进行思考,通过湿热灭菌之后,这些小(xiǎo)片断会变得更小(xiǎo)。有(yǒu)一些研究报道,这些极小(xiǎo)的片段有(yǒu)可(kě)能(néng)引起不良反应的,这是我们从湿热灭菌这个角度,能(néng)使工艺上的产品更能(néng)够符合市场的预期。
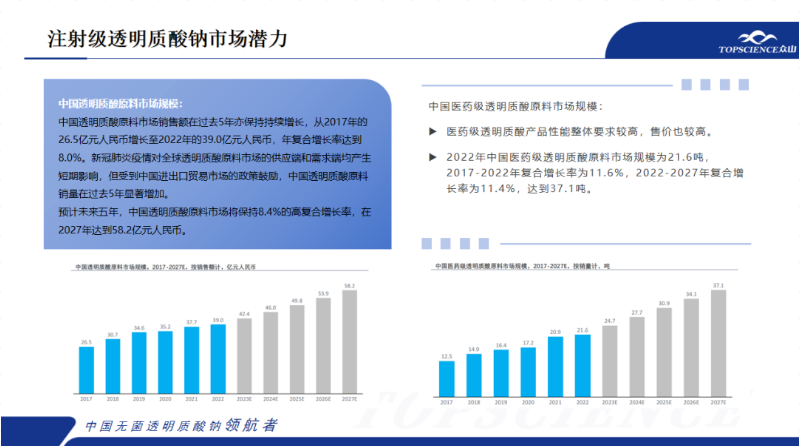
根据沙利文(wén)数据,预计未来五年,中國(guó)透明质酸原料市场将保持8.4%的高复合增長(cháng)率,在2027年达到58.2亿元人民(mín)币。2022年中國(guó)医药级透明质酸原料市场规模為(wèi)21.6吨,2017-2022年复合增長(cháng)率為(wèi)11.6%,2022-2027年复合增長(cháng)率為(wèi)11.4%,达到37.1吨。

从眼科(kē)到医美抗衰,市场对于透明质酸钠品质的需求越来越高,所以我们顺应时势推出了无菌透明质酸钠生产線(xiàn),更高程度满足了市场的需求。
对比传统的医药级透明质酸钠,无菌透明质酸钠有(yǒu)着显著优势,无菌透明质酸钠在质量管理(lǐ)、厂房设施、原料选用(yòng)、工艺无菌保障等方面要求格外严格,都是為(wèi)保证后面储存以及使用(yòng)过程中没有(yǒu)微生物(wù)的滋生。众山(shān)生物(wù)基于十多(duō)年发酵技术的积累,率先提出了中國(guó)首家无菌透明质酸钠車(chē)间。
探索未来
众山(shān)生物(wù)将不断提升产品品质和服務(wù)质量,积极研发创新(xīn),探索无限可(kě)能(néng),更多(duō)地為(wèi)透明质酸钠市场助力。












